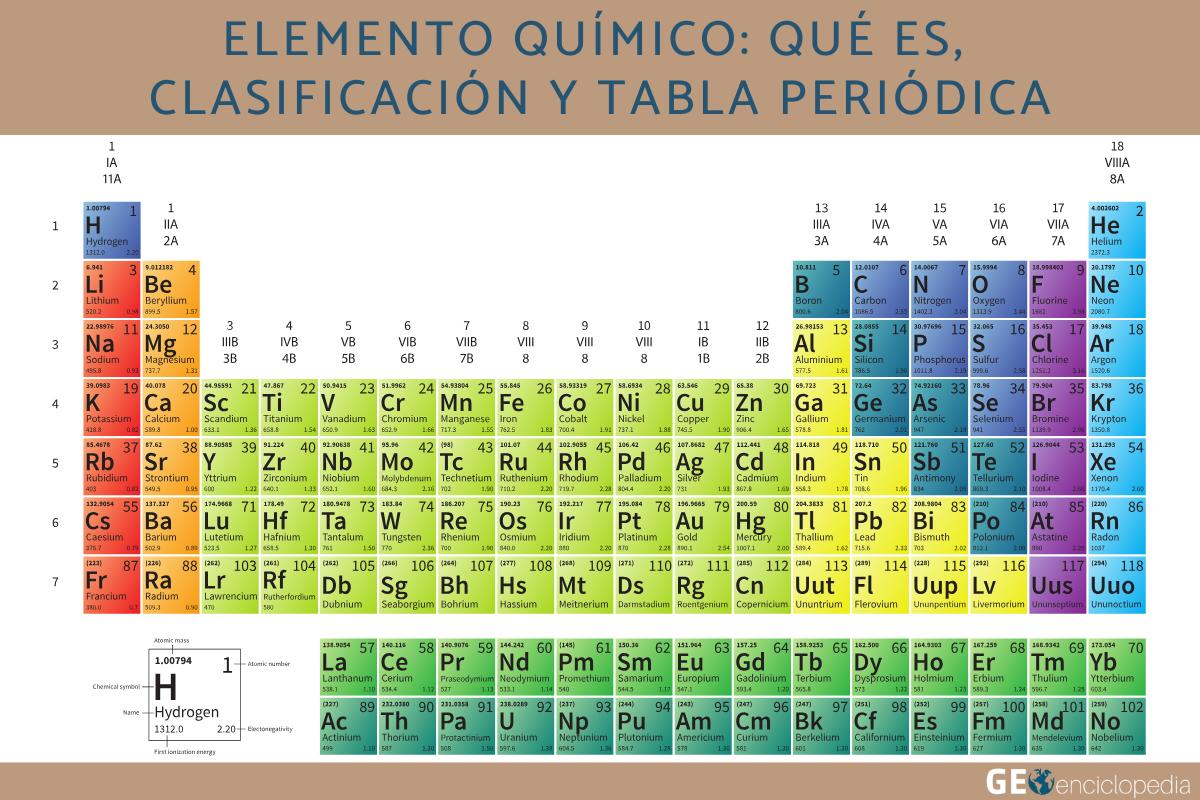
Elemento químico: qué es, clasificación y tabla periódica

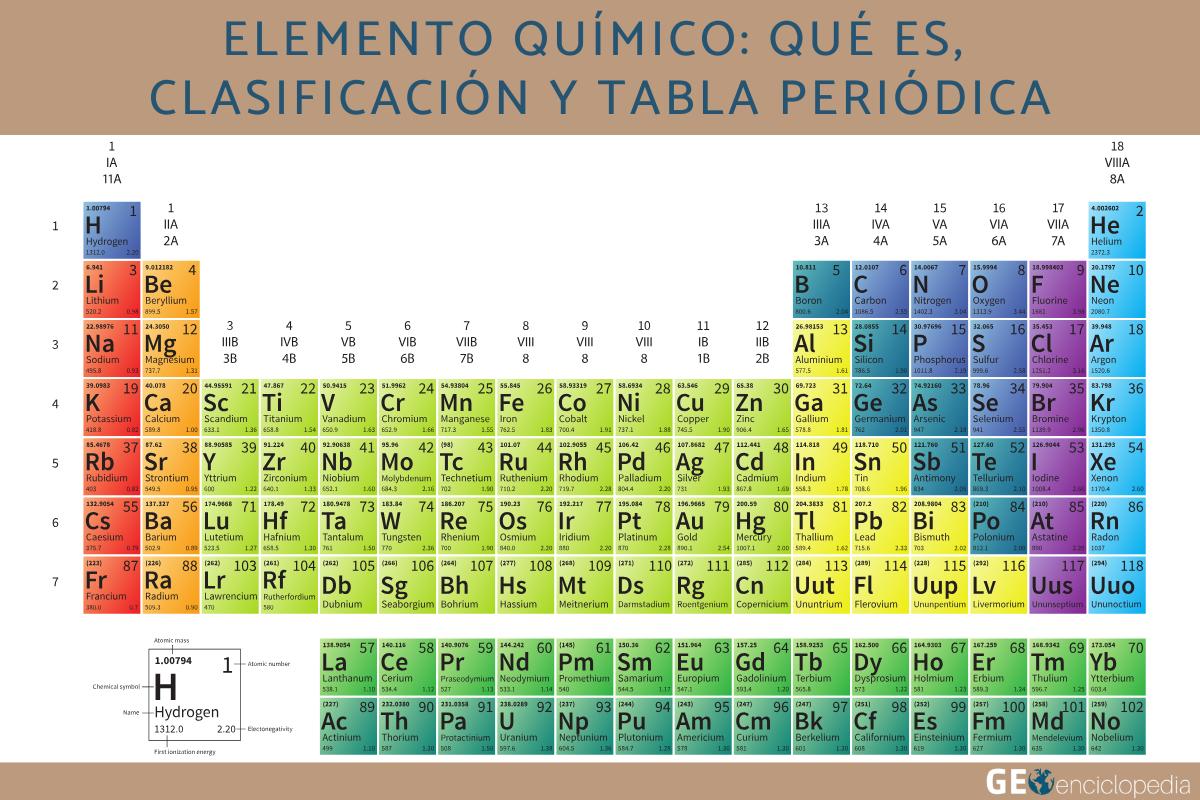
Un elemento químico es una sustancia pura compuesta por átomos con igual número de protones. Son los componentes fundamentales de la materia y no pueden descomponerse en sustancias más simples por medios químicos. Se clasifican en metales, no metales, metaloides, elementos representativos, de transición y gases nobles. Todos están organizados en la tabla periódica, dispuestos según su número atómico en filas (períodos) y columnas (grupos) que reflejan sus propiedades y comportamiento químico. Descubre qué es un elemento químico, clasificación y tabla periódica en este artículo de GEOenciclopedia.
¿Qué es un elemento en química o elemento químico?
Un elemento químico es una sustancia pura formada por átomos que tienen el mismo número de protones en su núcleo, conocido como número atómico. Este número es lo que distingue a un elemento de otro y define sus propiedades químicas y físicas. Los elementos son los componentes básicos de toda la materia y no pueden descomponerse en sustancias más simples mediante procesos químicos ordinarios.
Cada elemento posee un símbolo único, generalmente derivado de su nombre en latín o inglés, que lo representa en la tabla periódica. Por ejemplo, el oxígeno se simboliza con la letra "O" y el hidrógeno con la "H". Las propiedades de los elementos, como su reactividad, estado de agregación o capacidad de formar compuestos, se estudian dentro de la química para comprender la estructura y el comportamiento de la materia.
Ahora bien, ¿cuántos elementos químicos hay? Actualmente, la tabla periódica reconocida por la Unión Internacional de Química Pura y Aplicada (IUPAC) incluye 118 elementos. De ellos, algunos son naturales, presentes en la Tierra o en el espacio, mientras que otros han sido creados artificialmente en laboratorios mediante reacciones nucleares. Estos últimos suelen ser inestables y existen solo durante fracciones de segundo antes de desintegrarse.
¿Cómo es la clasificación de los elementos químicos?
Metales
Los metales constituyen la mayoría de los elementos. Se caracterizan por ser buenos conductores de calor y electricidad, tener brillo metálico y ser maleables y dúctiles. Suelen formar cationes al perder electrones y están presentes en aplicaciones como la construcción, la energía y la fabricación de herramientas.
No metales
Los no metales son menos abundantes en la tabla periódica, pero desempeñan un papel vital. Carecen de brillo, son malos conductores de electricidad y se encuentran en estados sólidos, líquidos o gaseosos a temperatura ambiente. Forman compuestos esenciales como el agua, los ácidos y las bases.
Metaloides
Los metaloides poseen propiedades intermedias entre metales y no metales. Pueden comportarse como conductores en ciertas condiciones y como aislantes en otras, lo que los hace indispensables en la industria de semiconductores y la electrónica.
Elementos representativos
Estos abarcan los grupos 1, 2 y del 13 al 18 de la tabla periódica. Incluyen metales, no metales y gases nobles. Sus propiedades son diversas, pero destacan por participar en la formación de gran variedad de compuestos químicos.
Elementos de transición
Ubicados en los grupos 3 al 12, estos metales son muy utilizados en la industria. Presentan varios estados de oxidación y suelen formar compuestos coloreados, además de ser esenciales en la catálisis.
Gases nobles
Son elementos muy estables debido a que poseen su capa externa de electrones completa. Se encuentran en la atmósfera en pequeñas cantidades y se utilizan en iluminación y procesos industriales específicos.
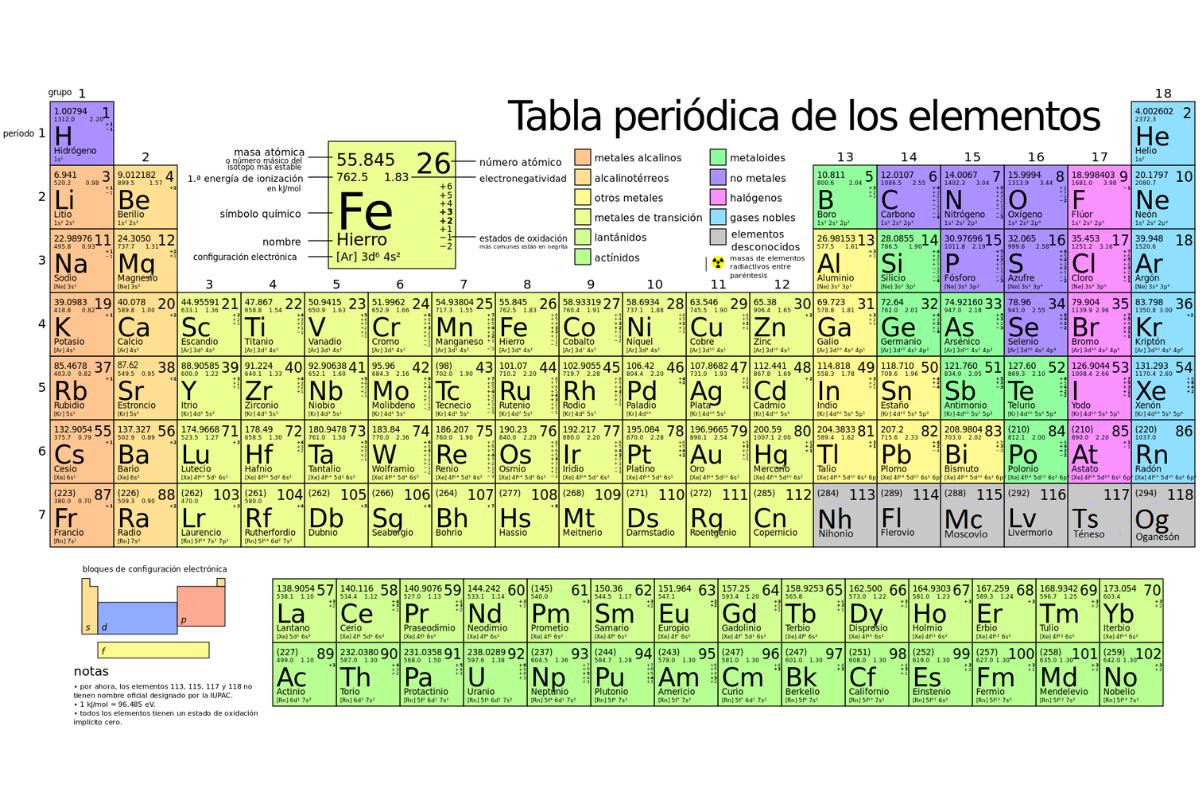
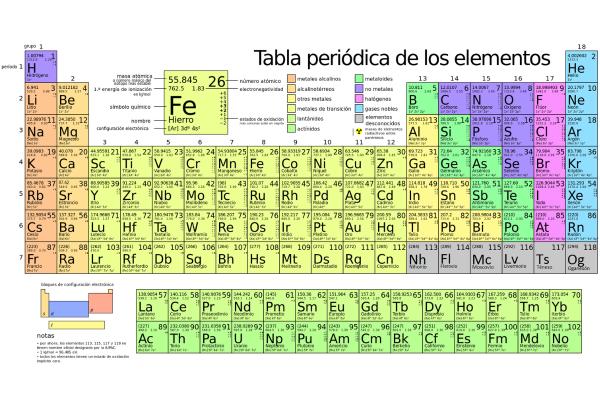
¿Cómo se organizan los elementos químicos en la tabla periódica?
La tabla periódica de los elementos químicos es una herramienta que organiza todos los elementos conocidos de manera lógica y ordenada, permitiendo comprender sus propiedades y relaciones. Su organización se basa principalmente en el número atómico, es decir, la cantidad de protones que posee cada átomo en su núcleo.
- Los elementos se disponen en filas horizontales llamadas períodos. Cada período refleja el nivel de energía principal en el que se encuentran los electrones de los átomos. A medida que se avanza de izquierda a derecha dentro de un mismo período, los elementos van aumentando de un protón en su núcleo y adquieren características químicas diferentes.
- También se organizan en columnas verticales llamadas grupos o familias. Los elementos de un mismo grupo comparten propiedades similares, ya que presentan el mismo número de electrones en su capa externa. Por ejemplo, los elementos del grupo 1 son los metales alcalinos, muy reactivos, mientras que los del grupo 18 son los gases nobles, caracterizados por su estabilidad química.
- Además, la tabla se divide en bloques (s, p, d y f), que indican el tipo de orbital en el que se encuentra el último electrón. Esta distribución permite identificar con facilidad si un elemento es un metal, un no metal o un gas noble, y facilita la predicción de su comportamiento en reacciones químicas.
¿Para qué sirven los elementos químicos?
Los elementos químicos son la base de toda la materia que nos rodea. Cada uno posee propiedades únicas que permiten su aplicación en distintos ámbitos de la vida diaria, la industria, la medicina y la tecnología. Comprender para qué sirven facilita entender su valor en el desarrollo humano y en el funcionamiento natural del planeta. Entre sus utilidades, podemos mencionar:
- Construcción de la materia: forman todo lo que existe, desde los objetos cotidianos hasta los seres vivos.
- Biología y salud: elementos como el oxígeno, el carbono, el hidrógeno y el nitrógeno son esenciales para la vida. Además, minerales como el calcio y el hierro cumplen funciones vitales en el cuerpo humano.
- Medicina: se utilizan en fármacos, tratamientos y equipos médicos. Por ejemplo, el yodo en desinfectantes y el cobalto en radioterapia.
- Energía: elementos como el uranio permiten generar electricidad en centrales nucleares, mientras que el hidrógeno se estudia como combustible limpio.
- Industria y tecnología: el silicio es fundamental en la fabricación de chips electrónicos y el cobre se emplea en cables de conducción eléctrica.
- Agricultura: nutrientes como el fósforo, el potasio y el azufre son clave para el crecimiento de las plantas.
- Ambiente: algunos elementos participan en ciclos naturales, como el oxígeno en la respiración y el carbono en el efecto invernadero.
¿Qué diferencia hay entre un elemento químico y un compuesto químico?
- Elemento químico: es una sustancia pura formada por átomos que tienen el mismo número de protones en su núcleo. No puede descomponerse en otras sustancias más simples mediante procesos químicos. Ejemplos de elementos son el oxígeno (O), el hierro (Fe) o el oro (Au). Cada elemento está representado en la tabla periódica con un símbolo específico.
- Compuesto químico: es una sustancia formada por la unión de dos o más elementos diferentes en proporciones fijas. Esta unión se da mediante enlaces químicos, ya sean iónicos o covalentes, lo que genera nuevas propiedades distintas a las de los elementos que lo conforman. Por ejemplo, el agua (H₂O) es un compuesto formado por hidrógeno y oxígeno, y la sal de mesa (NaCl) resulta de la unión del sodio y el cloro.
Si deseas leer más artículos parecidos a Elemento químico: qué es, clasificación y tabla periódica, te recomendamos que entres en nuestra categoría de Química.
- Elguero, J., Goya, P., & Román, P. (2019). La tabla periódica de los elementos químicos. Los libros de la catarata.
- Rivera, J. M. T. (2020). Historia de la tabla periódica de los elementos químicos. In Anales de la Real Academia de Doctores (Vol. 5, No. 2, pp. 241-259). Real Academia de Doctores de España.